Efeito dos glicocorticóides
-aumentam a produção de glicogênio assim como de aminoácidos, ác. gráxos e glicerol (substratos para gliconeogênese) => jejum prolongado
-reduzem sensibilidade dos tecidos à insulina. Logo, reduzem a captação de glicose, potencializando a secreção de insulina.
ações antiinflamatórias: bloqueiam ou retardam etapas do processo inflamatório
imunossupresoras: desativam linfócitos T e inibem produção de citocinas que ativam o sistema imunitário. O que é muito importante em doenças auto-imune para desaceleração da resposta imunitária.
-inibe formação do osso (em excesso, ocasionará osteoporose)
-inibe formação de colágeno
Mecanismos de ação
-por serem lipossolúveis, os glicocorticóides difundem-se com facilidade pela membrana plasmática, interagindo diretamente com o receptor.
-já no plasma, esse caráter lipofílico dificulta o transporte dessa molécula que é atuenuado pela associação a moléculas protéicas
Ritmo Circadiano
-são padrões diários de regulação do sono, energia e secreção de hormônios.
Os corticóides são sintetizados enquanto dormimos, tendo seu pico ao acordarmos e descre no decorrer no dia. Daí a importância de dormimos pelo ou menos 8h/dia.
curiosidade importante: o gráfico de tensão arterial acompanha o de corticóides porque com a síntese de mineralocorticóides enquanto dormimos, há o aumento de absorção do sódio no intestino o que acarreta no aumento de pressão arterial quando acordamos.
Esse quadro se agrava em países frios pois, com as baixas temperaturas, o metabolismo está muito lento, necessitando ainda mais de aumentar a tensão arterial para maior fluxo sanguíneo ao acordar.
Um outro ritmo circadiano é a relação insulina-glucagon.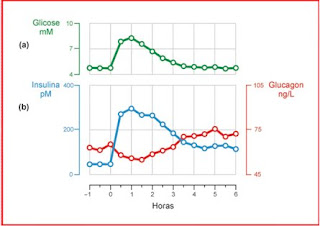
Num período de 0h (período absortivo) indica que a pessoa acabou de ingerir o alimento. Assim, no período pós-absortivo, nota-se que o nível de glicose no plasma se eleva rapidamente (principalmente se a alimentação da pessoa foi a base de carboidratos simples). Juntamente com a glicose, eleva-se a insulina que vai estimular a entrada da glicose nas células dos tecidos. Após esse período, verifica-se o decréscimo da taxa de glicose e de insulina indicando que está acontecendo o processo de fosforilação da glicose. A partir de 3h após a ingestão do alimento, a insulina plasmática está decaindo muito, o que estimula a secreção de glucagon pelo pâncreas (hormônio contra-regulatório da insulina). Altos níveis de glucagon no sangue estimulará a glicogenólise (fosforilação do glicogênio hepático para formação de glicose). Por isso que é recomendado que as pessoam se alimentem de 3 em 3h para manter a taxa metabólica do organismo.
Resposta ao estress
- o eixo hipotálamo(CRH)-hipófise(ACTH)-adrenal(glicocorticóides)
-Fatores que estimulam o cortisol (principal glicocorticóide): ansiedade, competição, depressão, exercício físico, hipoglicemia, queimaduras, exposição ao frio e hipertermia. Por isso que o cortisol é considerado o "hormônio do estress". Por exemplo, na TPM, ele não é o precursor mas é um importante coadjuvante desse quadro.
sexta-feira, 3 de julho de 2009
- Seminário de Corticóides e Hormônios da Tireóide - Apresentação Isabella Duarte
Postado por Isabella Duarte às 06:06 0 comentários
quinta-feira, 2 de julho de 2009
- Seminário de Corticóides e Hormônios da Tireóide - Apresentação Raquel Scafuto
- O que são corticóides?
Corticóides ou corticoteróides são o grupo de hormônios esteróides produzidos pelas glândulas supra-renais. Existem também derivados sintéticos. Eles tem diversas ações importantes no corpo, como por exemplo, na regulação metabólica de carboidratos, lipídios e proteínas, equilíbrio eletrolítico e hídrico corporal, capacidade funcional dos rins, na musculatura esquelética, no sistema nervoso, etc.
São produzidos no cortex da adrenal, em três regiões e formando três diferentes tipos: mineralocorticóides (região glomerulosa), androgênicos (região reticulada) e glicocorticóides (região fasciculada).
Sua síntese é regulada pelo hipotálamo (eixo H-H-SR), que libera ACTH-RH quando estimulado em situações de estresse, dor e do ritmo circadiano. O ACTH-RH liberado atua sobre a hipófise, estimulando a liberação de ACTH(adrenocorticotropina). E o ACTH estimula a liberação de corticóides pelas glândulas supra-renais.
Essa liberação é regulada pelo mecanismo de feedback negativo. Quando os níveis de corticóides estão elevados, ocorre um feedback negativo, que regula a liberação de ACTH-RH devido ao efeito inibitório da alta concentracão de corticóides.
- Colesterol
O ACTH é fundamental na produção de corticóides porque ele tem como função aumentar a capacitação de colesterol pelas células adrenais. E o colesterol é o precursor desses hormônios, e o principal precursor da vitamina D.
Ele é adquirido na dieta a partir da gordura animal e é também sintetizado no retículo endoplasmático de alguns órgãos do nosso corpo. Ele é sintetizado a partir do Acetil-CoA (sequência de 30 reações enzimáticas), que sofre clivagem, removendo-se um fragmento de seis carbonos, o isocapropaldeído, e formando pregnenolona, que é indispensável na síntese desses hormônios esteróides.
A partir desse ponto a pregnenolona pode sofrer diversas oxidações ou hidroxilações, dando origem aos mineralocorticóides, androgênicos e glicocorticóides.
- Mecanismos de ação
Depois de prontos, esses hormônios tem que agir nas células-alvo e fazer com que elas executem determinadas funções. Os hormônios esteróides utilizam um mecanismo de ativação de genes, que vai controlar a taxa de síntese protéica.
Esse mecanismo funciona da seguinte forma:
Os hormônios entram na célula e se ligam a um receptor, que passa da forma inativa para a forma ativa. Este complexo esteróide-receptor entra no núcleo da célula e, devido a mudanças conformacionais, consegue se fixar e ativar porções específicas do DNA, especificando a transcrição para o RNA mensageiro, que vai para o citoplasma e determina quais serão as proteínas sintetizadas, que vão influenciar em atividade também específicas.
Os receptores de glicocorticóides são chamados GR ou GR tipo II e dos mineralocorticóides, MR mas que por ter forte homologia com o GR, é conhecido como GR tipo I.
- Mineralocorticóides
O principal é a aldosterona, produzido pela adrenal. Outros menos importantes são a desoxicorticosterona e a corticosterona. Existem também derivados sintéticos, um exemplo é o fludrocortisona.
São responsáveis pelo controle eletrolítico, ou seja, regulam a homeostasia de sódio e potássio. Nos néfrons do túbulo contornado distal e no ducto coletor ocorre a reabsorção de sódio e a excreção de potássio.
Com a absorção de sódio, cloretos também são absorvidos, havendo a formação de NaCl por exemplo. Com a formação de sais, água também é absorvida por osmose, o que aumenta o volume do líquido extra-celular.
Também causa a secreção de ions de hidrogênio em troca de absorção de sódio.
O ACTH e o excesso de potássio são estimulantes para a produção de aldosterona, mas o sistema renina-angiotensina é o principal mecanismo de controle da produção de aldosterona.
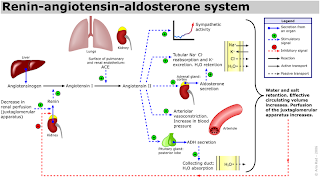
- Sistema renina-angiotensina
O sistema renina-angiotensina funciona da seguinte maneira: o angiotensinogênio é produzido no fígado, que requer de glicocorticóides e estrógeno. A enzima renina é produzida nos rins.
A renina converte o angiotensinogênio em agiostensina I, que é convertida a agiostensina II pela ação da enzima de conversão (ECA), produzida principalmente nos epitélios pulmonares.
A angiostensina II é utilizada em diversos processos. Mas nesse estudo, é importante porque ativa diretamente a bomba eletrogênica de prótons, que troca Na+ por H+, e indiretamente ativando a secreção de aldosterona, que vai ativar a bomba de Na+/K+.
- Andrógenos
Hormônios como o DHEA, DHEA-S e androstenediona são relativamente fracos e depois se convertem a testosterona.
A produção de andrógenos ocorre em pequenas quantidades nas glândulas supra-renais tanto nos homens quanto nas mulheres.
Nos homens, a grande necessidade de testosterona é suprida pela produção dos testículos.
Nas mulheres, permite o desenvolvimento de pelos axilares e pubianos. Pode causar sinais de masculinização quando ocorre uma hipersecreção hormonal.
Postado por Raquel Scafuto às 16:05 0 comentários
quarta-feira, 1 de julho de 2009
- Seminário de Corticóides e Hormônios da Tireóide – Apresentação de Isabelle Nolasco
DOENÇA DE ADDISON:
* É uma doença caracterizada pela destruição do córtex da glândula supra-renal, que produz corticóides nas zonas glomerulosa, fasciculada, e reticular, portanto leva a deficiência crônica de corticóides.
* Existem dois tipos:
- TIPO I: afeta mais crianças do sexo feminino e é caracterizada pela doença de Addsison associada ao hiperparatireoidismo e candidíase mucocutânea.
- TIPO II: afeta mais mulheres com idade entre 20 e 50 anos e é caracterizada pela associação da Doença de Addison, a tireoidite de Hashimoto, e ao Diabetes mellitus I.
* Pode ser causada ou influenciada por vários fatores, como Doenças infecciosas (por exemplo, tuberculose); por agentes oportunistas na AIDS que causam a destruição do córtex das adrenais; por hemorragias nas supra-renais; defeitos congênitos de alguma enzima necessária na síntese de corticóides (por exemplo, a 21 hidroxilase, que é a deficiência mais freqüente nesses casos); por drogas usadas no tratamento da Síndrome de Cushing. A doença de Addison tambpem pode ser auto-imune.
*Os sintomas decorrentes da doença são reflexos da falta de corticóides no organismo:
- Concentração de pigmentos nos seios, nas articulações, ou em cicatrizes: A secreção de ACTH estimula a secreção de outro hormônio: o MSH – hormônio melanócito estimulante. A baixa concentração de corticóides, estimula a hipófise a estar secretando sempre ACTH apesar da deficiência da glândula supra-renal, que não vai responder ao estímulo...
- Hipotensão Arterial: A aldosterona tem papel importante na regulação de sódio e potássio no sangue. Como este hormônio é um mineralocorticóide e está deficiente, o Sódio vai estar indo embora, e junto com ele água. A desidratação também é outro sintoma da Doença de Addison
* A doença de Addison é rara e atinge mais as mulheres. Quando foi descoberta, em 1855, a causa que mais afetava homens era a tuberculose.
* Curiosidade: O Presidente John F. Kennedy, conseguiu esconder durante anos sua doença. Ele Tinha Doença de Addison e levava uma vida aparentemente normal (apesar de tomar vários remédios por dia). Ele não foi o único presidente americano a sofrer com a Doença. Fraklin D. Roosevelt também mantinha a doença em segredo.
- fofoca na íntegra no site:
www.portal.alert-online.com/?key=680B3D50093A6A002E42140A321A2A5C0B683E0A7607517E61587A
SÍNDROME DE CUSHING:
A síndrome de Cushing é decorrente da exposição excessiva e continuada a glicocorticóides, e pode ser: Endógena: hiperplasia das zonas fasciculada e reticular, levando a secreção excessivade corticóides.Devido a anormalidades/tumores na Hipófise levando a um aumento excessivo de ACTH ou CRH, ou exógena: devido a administração excessiva de glicocorticóides ou ACTH em algum tratamento.
A obesidade, stress e o alcoolismo também pode causar freqüente aumento na produção de cortisol.
Os sintomas decorrentes da doença são reflexos do excesso de corticóides no organismo:
- O cortisol inibe a síntese protéica, e o colágeno faz parte de 30% das proteínas do nosso corpo, sendo responsável pela sustentação. Um sintoma decorrente desse fato é a pele fina e a fragilidade na parede dos capilares sanguíneos. Uma consequência do extravasamento de sangue dos capilares são as Equimoses (causando manchas roxas na pele) e as Estrias avermelhadas onde ocorreu a lesão dos capilares.
- O excesso de cortisol também pode levar a um quadro de osteoporose (os osteoblastos sintetizam a matriz óssea, porém o colágeno é um componente desta; além de ser um problema na síndrome de Cushing, é uma preocupação para o profissional de saúde que receita tratamentos com cortisol a longo prazo);
- Obesidade centralizada, principalmente no rosto, e na barriga.
Postado por Isabelle Nolasco às 18:19 0 comentários
- Seminário de Hormônios da Tireóide e Corticóides - Apresentação Rafaella Dusi
As doença da tireóide são mais comuns em mulheres, já que o estrógeno estimula uma via que aumenta a produção de proteínas transportadoras de T3 e T4.
HIPERTIREOIDISMO: caracterizado pelo aumento das concentrações de T3 e T4.
O excesso dos hormônios tireoidianos aceleram o metabolismo e causam diversos sintomas. Alguns deles, e suas explicações serão citados a seguir:
O BÓCIO ( aumento da glândula) é causado por essa maior produção de hormônios, a PERDA DE PESO é observada pois o a lipólise e a proteólise ficam estimuladas. Essa lipólise estimulada também leva a uma diminuição do COLESTEROL. SUDORESE e HIPERTERMIA ocorrem devido à uma maior produção de calor. No fígado, esses hormônios em excesso aumentam a DEGRADAÇÃO DE ESTERÓIDES. A pessoa com Hipertireoidismo tem TREMORES e INSÔNIA pois altos níveis de T3 e T4 aumentam a excitabilidade neuromuscular. IRREGULARIDADES MENSTRUAIS também compõe o quadro dos sintomas, já que os hormônios da tireóide estão intimamente ligados aos hormônios que regulam os ciclos menstruais.
Estudos apontam como principal causa do Hipertireoidismo, uma doença auto imune, a DOENÇA DE GRAVES. Nessa doença os linfócitos B produzem uma imunoglobulina, o TSI (imunoglobulina estimulante da tireóide) e ela se acopla ao receptor de TSH (hormônio estimulante da tireóide), competindo pelo mesmo sítio ativo. O TSI estimula a glândula a uma produção exagerada de T3 e T4.
A EXOFTALMIA é um sintoma característico da Doença de Graves.
O tratamento mais comum para o Hipertireoidismo é feito com IODO RADIOATIVO. Ele ocorre da seguinte forma: a glândula absorve o iodo que foi inserido na circulação e esse iodo atinge a glândula provocando uma destruição lenta e parcial/total dela. Isso leva a diminuição do tamanho da glândula, regulando o quadro.
HIPOTIREOIDISMO:caracterizado por uma produção deficiente de hormônios tireoidianos. Sem a quantidade adequada desse hormônios, o metabolismo fica mais lento. A menor concentração desses hormônios gera os seguintes sintomas:
O doente tem uma maior INTOLERÂNCIA AO FRIO, pois há uma menor produção de calor. Há uma redução na lipólise, portanto as pessoas com hipotireoidismo tem SOBREPESO e aumento do COLESTEROL, isso aumenta o risco do doente
desenvolver ARTEROSCLEROSE. A HIPOGLICEMIA também é sintoma, pois a glicogenólise e a gliconeogênese ficam desestimuladas com os baixos níveis de T3 e T4. DEPRESSÃO e COSTIPAÇÃO são causados respectivamente por uma menor excitabilidades neuromuscular e uma menor mobilidade gastrointestinal. A menor mobilidades do trato gastrointestinal também causa freqüentemente o REFLUXO.
Os acometidos pelo hipotireoidismo apresentam algumas vezes inchaço, pois há uma diminuição na filtração dos glomérulos renais e com isso RETENÇÃO DE SAL E ÁGUA.
As causas mais comuns do desenvolvimento do hipo são o tratamento para hipertireoidismo, cirurgia de retirada da glândula e a DOENÇA DE HASHIMOTO.
A doença de Hashimoto é também uma doença auto imune, onde o sistema imunológico ataca a glândula e suas células vão sento destruídas, assim a produção de T3 e T4 é comprometida. Como defesa, as células que ainda não foram destruídas tentam uma produção exagerada e isso causa o BÓCIO.
O tratamento é feito com reposição hormonal de T4 para suprir as necessidades do organismo. O T4 é a forma escolhida pois no organismo ele é convertido em T3.
Postado por Rafaella Dusi às 17:55 0 comentários
- Famosas com hipotireoidismo


Postado por Raquel Scafuto às 17:51 1 comentários
- Harvey William Cushing
Foi graças a sua experiência médica, e de técnicas cirúrgicas para operações cerebrais desenvolvidas por ele, que a neurocirurgia se tornou uma disciplina cirúrgica nova e autônoma. Devido às melhoras nas técnicas cirúrgicas, a qualidade de vida de pacientes pós-operados aumentou consideravelmente. Por isso, se tornou um dos maiores líderes científicos
Em 1912, Harvey William Cushing descobriu uma síndrome endocrinológica causada pelo mau funcionamento da glândula tireóide, descrevendo essa síndrome em um livro publicado chamado "The Pituitary Body and Its Disorders" e imortalizando seu nome na história da medicina.
Fontes:
http://www.cerebromente.org.br/n02/historia/cushing_p.htm
http://daphne.palomar.edu/ccarpenter/harvey_william_cushing.htm
http://www.geocities.com/wrcushing/h/harvey1869.html
Postado por Raquel Scafuto às 17:18 0 comentários
Marcadores: D
sexta-feira, 26 de junho de 2009
- Sensibilidade aos Glicocorticóides
Os GLICOCORTICÓIDES exercem um papel importante em vários órgãos e sistemas, participando da regulação fisiológica e da adaptação às situações de stress, sendo a maioria dos efeitos destes hormônios mediada pela interação com os receptores glicocorticóides (GR). Os glicocorticóides são regulados pelo eixo hipotalâmico-hipofisário-adrenal, influenciado por fatores como o ritmo circadiano, o stress e o feedback negativo.
Vários fatores influenciam a cascata de eventos que leva à modulação da sensibilidade aos glicocorticóides:
-a concentração hormonal
-a biodisponibilidade do glicocorticóide
-a afinidade do receptor para ligação hormonal
-a densidade intracelular de GR
-a fosforilação do GR
-a translocação nuclear do receptor ativado
-a interação com o elemento responsivo ao glicocorticóide (GRE)
-os fatores de transcrição
e PRINCIPALMENTE:
-ATIVAÇÃO de seus receptores.
O receptor glicocorticóide é uma exceção, pois na ausência de ligação ao cortisol, encontra-se inativo no citoplasma, estabilizado por um complexo protéico. Essa estrutura compreende, pelo menos, uma molécula do receptor e outras três proteínas específicas e permitem que o receptor adquira uma conformação tridimensional adequada para a sua ligação ao hormônio.
Os estados de resistência ou de hipersensibilidade ao glicocorticóide são observados, em doenças inflamatórias auto-imunes e na síndrome metabólica. O reconhecimento destes fatores contribui para uma melhor compreensão tanto do fenótipo clínico e da evolução destas doenças quanto da resposta terapêutica com glicocorticóide.
bibliografia: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0004-27302006000600003&lng=pt&nrm=iso&tlng=pt
Postado por Isabella Duarte às 18:43 0 comentários